Calciumcarbonaat
Calciumcarbonaat | ||||
Structuurformule en molecuulmodel | ||||
 | ||||
Structuurformule van calciumcarbonaat | ||||
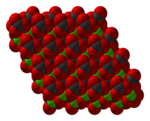 | ||||
Kristalstructuur van calciumcarbonaat | ||||
 | ||||
Calciumcarbonaat in poedervorm | ||||
Algemeen | ||||
Molecuulformule (uitleg) | CaCO3 | |||
| Andere namen | kalksteen, aragoniet, calciet, aeromatt, akadama, albacar, albafil, albaglos, atomite, AX 363, BF 200, brilliant 15, brilliant 1500, britomya, calcene, calcicoll, calcidar 40, calcilit, calmos, calmote, calofil, calofort, calopake, calseeds, caltec, carbium, durkal, zuiver krijt | |||
| Molmassa | 100,1 g/mol | |||
| SMILES | C([O-])(=O)[O-].[Ca+2] | |||
| CAS-nummer | 471-34-1 | |||
| EG-nummer | 207-439-9 | |||
| Beschrijving | wit poeder | |||
| Vergelijkbaar met | calciumbicarbonaat, calciumoxide, gips, natriumbicarbonaat, natriumcarbonaat | |||
LD50 (ratten) | 6450 mg/kg | |||
Fysische eigenschappen | ||||
| Aggregatietoestand | vast | |||
| Kleur | wit | |||
| Dichtheid | 2,93 g/cm³ | |||
| Smeltpunt | (ontleedt bij 899°C) 1339 °C | |||
| Onoplosbaar in | water | |||
Geometrie en kristalstructuur | ||||
| Kristalstructuur | tetragonaal | |||
Waar mogelijk zijn SI-eenheden gebruikt. Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | ||||
| ||||
Calciumcarbonaat (CaCO3) is het koolzure zout van calcium.
Inhoud
1 Voorkomen
2 Eigenschappen
3 Toepassingen
3.1 Als bouwmateriaal
3.2 In de landbouw
3.3 In voeding en geneeskunde
3.4 In industriële toepassingen
Voorkomen
Calciumcarbonaat komt in de natuur veel voor als het mineraal calciet. Het sedimentair gesteente kalksteen en de metamorfe vorm hiervan, marmer, zijn grotendeels uit calciet opgebouwd. In de natuur is calciet meestal gedeeltelijk vervuild met magnesiumionen, die in het kristalrooster van calciet calciumionen kunnen vervangen. Een instabiele polymorf van calciet is aragoniet. Van heel wat zeedieren is het skelet uit aragoniet opgebouwd. Nadat organismen met aragonietskeletten sterven sedimenteert hun skelet. Via rekristallisatie wordt het aragoniet weer calciet. De minst stabiele vorm van calciumcarbonaat is vateriet. Deze is in de natuur vrijwel niet te vinden, omdat de transformatie van vateriet naar calciet binnen een etmaal volbracht is.
De schaal van eieren en de schelp van slakken en schelpdieren bestaat grotendeels uit calciumcarbonaat. Het is ook een versterkend mineraal in de schalen van heel wat schaaldieren en insecten. Chemisch gezien is het calciumcarbonaat dat in de natuur voorkomt verontreinigd met allerlei andere stoffen.
In het huishouden kent men calciumcarbonaat als een van de componenten in ketelsteen.
Eigenschappen
Calciumcarbonaat is een zout en dus een ionofore stof. In zuivere toestand is het een witte vaste stof, die slecht oplosbaar is in water. In zuren is de stof wel oplosbaar, doordat zij ontleedt (koolstofdioxide is immers een gas):
- CaCO3 + 2 H3O+ ⟶ Ca2+ + 3 H2O + CO2{displaystyle {rm {CaCO_{3} + 2 H_{3}O^{+} longrightarrow Ca^{2+} + 3 H_{2}O + CO_{2}}}}
Het lage ontledingspunt (899°C) in vergelijking met het smeltpunt (1339°C) heeft te maken met het feit dat bij de ontledingstemperatuur de evenwichtsdruk van koolstofdioxide boven calciumcarbonaat de standaarddruk bereikt. De verbinding wordt dan omgezet in calciumoxide (CaO). Door ervoor te zorgen dat het gasvormige koolstofdioxide niet kan ontsnappen (zoals in een drukreactor) kan het smeltpunt van calciumcarbonaat bereikt worden.
Het kristalrooster van calciumcarbonaat is trigonaal (calciet) of orthorombisch (aragoniet).
Toepassingen
Als bouwmateriaal
Calciumcarbonaat wordt veel als bouwmateriaal gebruikt. Het vindt toepassingen als structureel element (tand) en als decoratief element. Kalksteen bevat vaak goed herkenbare fossielen. De kalk in kalksteen is immers afkomstig van de schalen van grote of kleine schelpdieren).
In de landbouw
In de landbouw wordt calciumcarbonaat onder de naam kalk gebruikt als bodemverbeteraar. De kalk neutraliseert de aanwezige zuren met zijn basisch carbonaation en verhoogt zo de pH. Hiervoor worden zowel kalkmeststoffen met magnesium gebruikt (Dolokal en Magkal) als calciumcarbonaat afkomstig van Limburgse mergel (Limkal en Vitakal). Ook een restproduct dat vrijkomt bij de productie van bietsuiker en dat calciumcarbonaat schuimaarde (Betacal) bevat, wordt in de landbouw afgezet. Dolokal en Magkal bevatten zo'n 80% kalk (CaCO3) en 19% magnesiumcarbonaat (MgCO3); dolomiet respectievelijk 60% en 8%.
Calciumcarbonaat is opgenomen in de Lijst van pesticiden die door de Europese Unie zijn toegelaten.
In voeding en geneeskunde
Het mineraal heeft een grijswit pigment en is binnen de Europese Unie goedgekeurd als een voedingskleurstof met het E-nummer E170(i). Het wordt bijvoorbeeld als oppervlaktekleuring gebruikt voor de witte "schimmel" bij verschillende soorten droge worsten. Het wordt ook gebruikt als oplosmiddel voor tabletten. Calciumcarbonaat is bijvoorbeeld het voornaamste bestanddeel van maagtabletten. Het wordt tevens gebruikt bij het ontzuren van wijn en rabarber (in poedervorm, genaamd krijtpoeder of neerslagkalk), en als stabilisator voor ingeblikt fruit. Verder wordt het gebruikt als een antiklontermiddel voor zout, en als verdikkingsmiddel.[1] In sommige soorten kauwgom wordt calciumcarbonaat als vulstof gebruikt.
In industriële toepassingen
In papierproductie voor het coaten van papier, als vulstof in (plastisol)lijmen en in polyurethaan.
| Zie de categorie Calcium carbonate van Wikimedia Commons voor mediabestanden over dit onderwerp. |
Bronnen, noten en/of referenties
|
